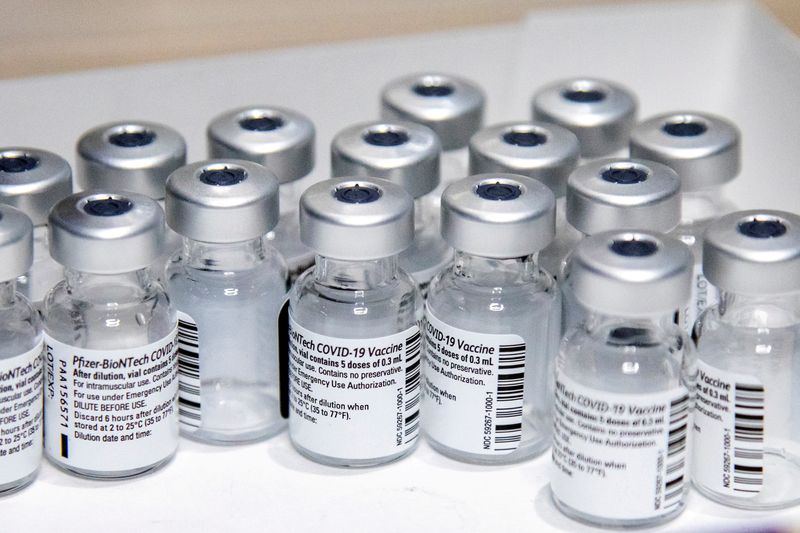
La nueva fórmula aumentó más de 10 veces los anticuerpos contra la variante respecto de la dosis original, según anunció la compañía. La FDA se reúne mañana para debatir la actualización de las vacunas.
Las empresas biotecnológicas Pfizer y BioNTech anunciaron que su vacuna diseñada específicamente contra la variante Ómcron del coronavirus es segura, eficaz y genera una elevada respuesta inmune. Las compañías hicieron el anuncio unos días antes de que los organismos reguladores de salud debatan si deben ofrecer a los estadounidenses vacunas de refuerzo actualizadas para el próximo otoño del hemisferio norte (a partir de septiembre de este año).
Pfizer y su socio BioNTech estudiaron dos maneras diferentes de actualizar su fórmula: una vacuna monovalente que se dirige sólo a Ómicron y una vacuna bivalente que combina la vacuna original y añade la protección frente a Ómicron.
Además, analizaron si debían mantener la dosis estándar actual —30 microgramos— o duplicar la potencia de las inyecciones.
Los sublinajes de Ómicron (BA.2, BA.4, BA.5) son aún más transmisibles y se han extendido ampliamente a nivel global. Las vacunas que se utilizan actualmente en los Estados Unidos y en el resto del mundo aún ofrecen una protección fuerte contra la enfermedad grave por COVID-19 y la muerte, sobre todo si las personas han recibido una dosis de refuerzo.
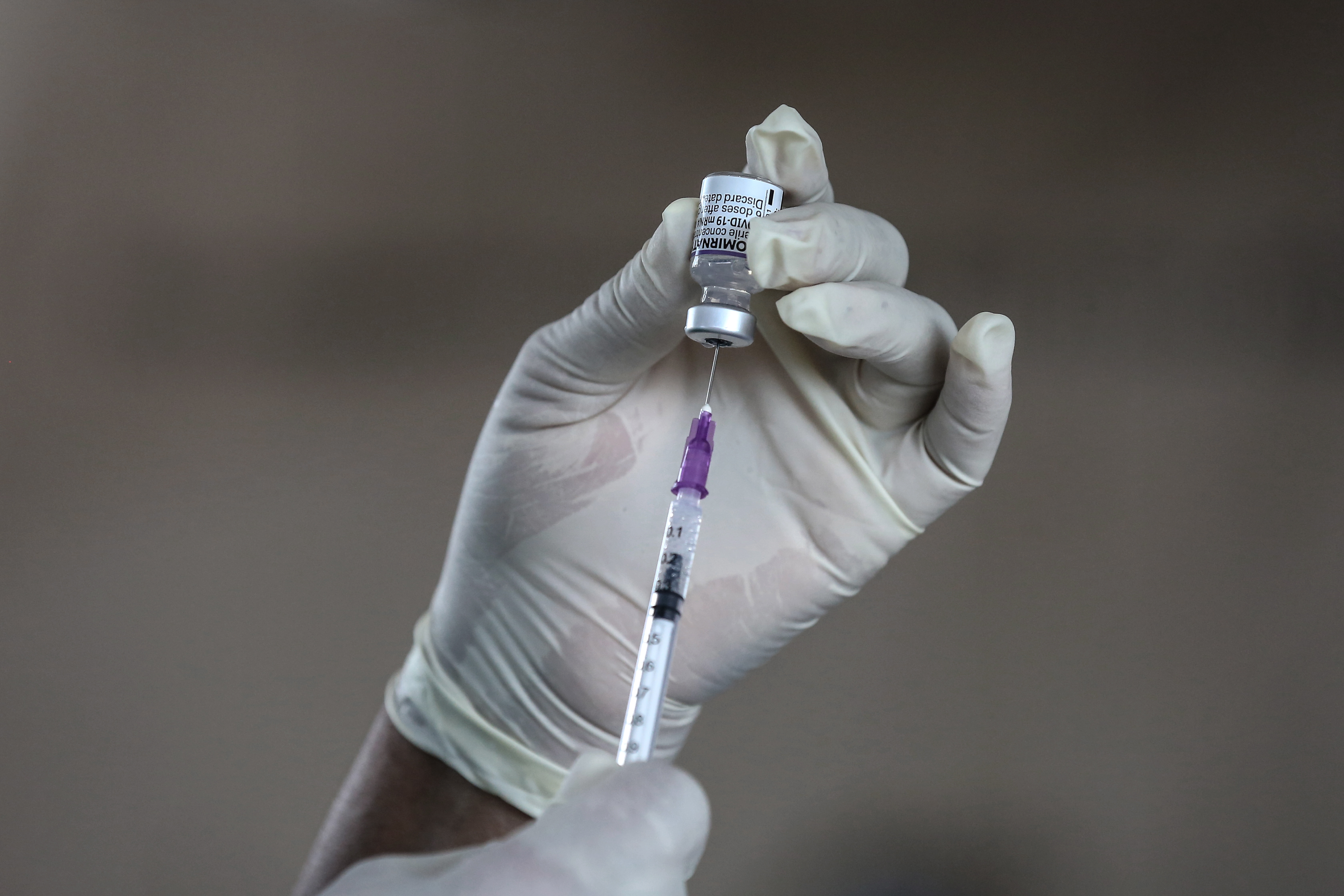
Sin embargo, estas fórmulas fueron diseñadas para combatir a la cepa original del coronavirus, detectada en Wuhan en diciembre de 2019, y su eficacia frente a la infección disminuyó de manera notable tras la aparicón de la variante Ómicron, que tiene alta transmisibilidad.
En el estudio realizado con 1.234 adultos de mediana edad y mayores que ya habían recibido tres dosis de la vacuna, Pfizer afirmó que, según los datos del ensayo de fase 2/3, ”una dosis de refuerzo de ambas vacunas candidatas adaptadas a Ómicron provocó una respuesta inmunitaria sustancialmente mayor contra Omicron BA.1 en comparación con la vacuna COVID-19 actual. La sólida respuesta inmunitaria se observó en los dos niveles de dosis en investigación, 30 µg y 60 µg.
“A partir de estos datos, creemos que tenemos dos candidatos muy fuertes adaptados a Ómicron que provocan una respuesta inmunológica sustancialmente más alta contra Ómicron que la que hemos visto hasta la fecha”, dijo en un comunicado el director general de Pfizer, Albert Bourla.
El refuerzo de Pfizer diseñado específicamente para la variante Ómicron provocó la respuesta inmunitaria más fuerte contra esa variante. Sin embargo, muchos expertos afirman que la combinación de vacunas podría ser el mejor enfoque, ya que conservaría los beneficios probados de la vacuna COVID-19 original y añadiría una nueva protección contra la variante Ómicron.
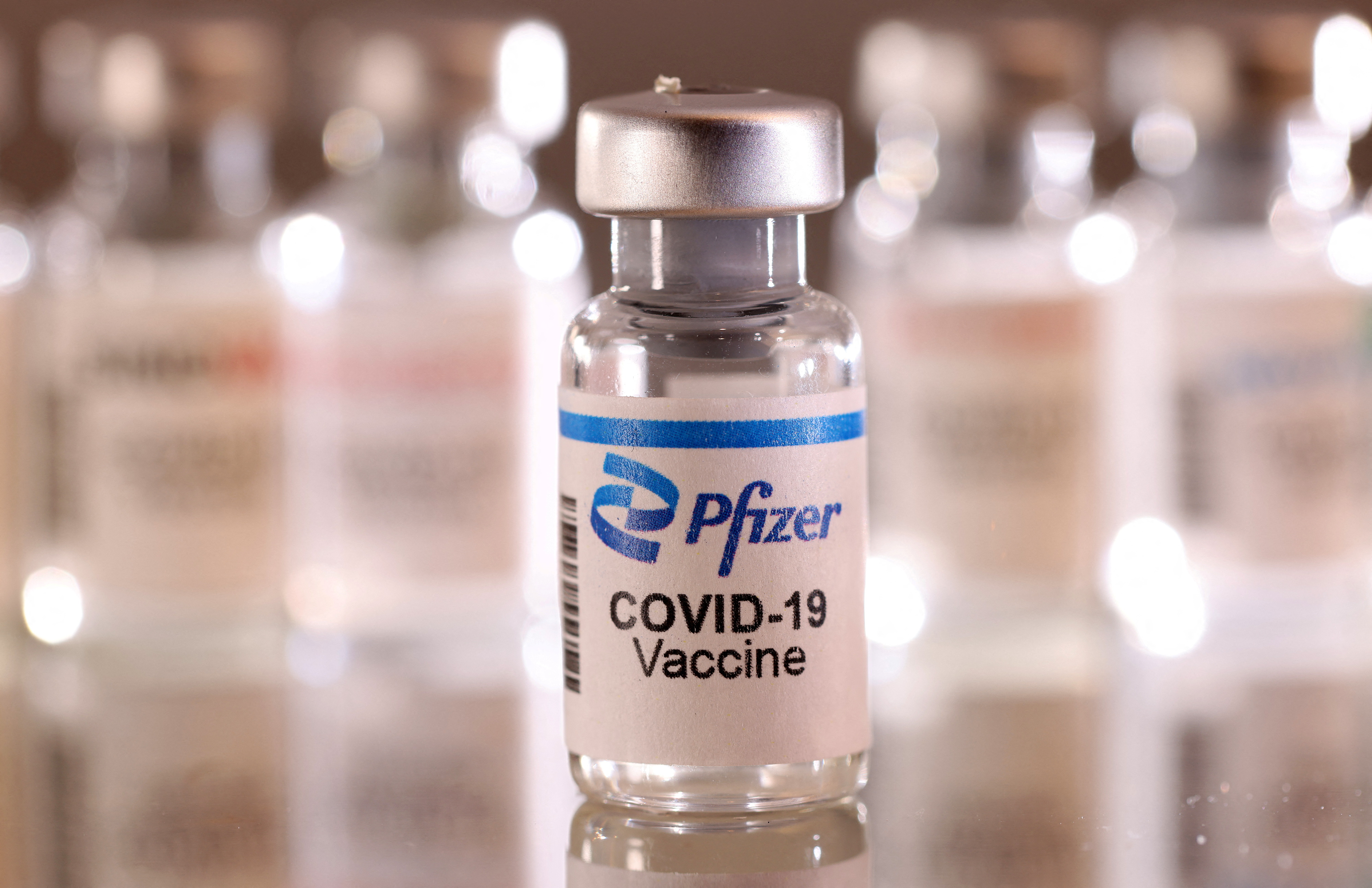
Un mes después de la aplicación, una dosis de refuerzo del candidatos monovalentes adaptados de Ómicron (30 µg y 60 µg) aumentó los anticuerpos frente a Omicron BA.1 entre 13,5 y 19,6 veces por encima de los niveles de la dosis previa al refuerzo. Asisimo, una dosis de refuerzo de los candidatos bivalentes adaptados a Omicron aumentó los anticuerpos entre de 9,1 a 10,9 veces.
Además, las compañías destacaron que los estudios preliminares de laboratorio demostraron que las vacunas modificadas también producen anticuerpos capaces de combatir a los sublinajes genéticamente distintos de Ómicron, denominados BA.4 y BA.5.
“Los datos muestran la capacidad de nuestras vacunas candidatas monovalentes y bivalentes adaptadas a Ómicron para mejorar significativamente las respuestas de neutralización de anticuerpos específicas de variantes”, dijo Ugur Sahin, CEO y cofundador de BioNTech y añadió: “Ómicron tiene sublinajes en evolución reciente que han superado a BA.1 y exhiben una tendencia creciente para el escape inmunológico. Por lo tanto, permaneceremos atentos y estamos preparados para adaptar rápidamente nuestras vacunas candidatas adaptadas a los sublinajes emergentes si los datos epidemiológicos y de laboratorio lo sugieren”.
“Estos resultados se comparten con la Administración de Alimentos y Medicamentos de EE. UU. (FDA) y la Agencia Europea de Medicamentos (EMA) antes de las próximas discusiones con el Comité Asesor de Vacunas y Productos Biológicos Relacionados (VRBPAC) de la FDA el 28 de junio y con la Coalición Internacional de Medicamentos. Autoridades Reguladoras (ICMRA) el 30 de junio”, concluyó el comunicado de las empresas. Desde mañana, las autoridades regulatorias de EEUU analizarán los detalles de las vacunas que se aplicará en el próximo otoño del hemisferio norte.
INFOBAE
ACERCA DEL CORRESPONSAL
REDACCIóN CENTRAL
Prensa Mercosur es un diario online de iniciativa privada que fue fundado en 2001, donde nuestro principal objetivos es trabajar y apoyar a órganos públicos y privados.
- ★Estas fotos no son de la festividad de Candelaria del Perú, fueron tomadas en Bolivia
- ★Paraguaná | Choferes insisten en ajuste del precio del pasaje
- ★EXPERIENCIA QUEEN LLEGA A SANTA CRUZ: El más grande tributo a QUEEN, Sábado 14 en Casa Grande
- ★Bonificaciones IVSS 2026: Fechas Confirmadas y Nuevos Montos
- ★Bonos Pensionados Marzo 2026: Lista actualizada y montos oficiales Patria